信念医药血友病基因疗法获国家药监局临床试验批准,为中国首个静脉给药的罕见病基因疗法
2021年08月06日
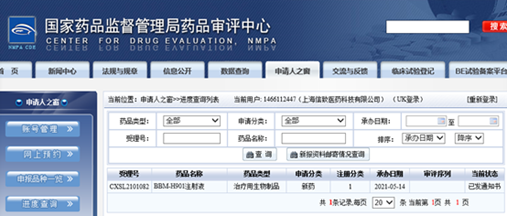
2021年8月6日,信念医药全资子公司上海信致医药科技有限公司自主研发的BBM-H901注射液(适用于预防血友病B成年男性患者出血的AAV基因治疗药物)获得国家药品监督管理局(National Medical Products Administration, NMPA)的药物临床试验批准,将正式启动注册临床试验。这是国内第一个获批进入注册临床试验的静脉给药血友病AAV基因治疗药物,也是国内第一个静脉给药的罕见病基因疗法。
信念医药首席执行官郑静表示,“如果将小分子药物、抗体药物称为生物医药的前两次革命,基因治疗被视为将引领生物医药的第三次产业革命。经过多年的技术积累,基因治疗产业市场规模增长迅速,辉瑞、诺华、强生等大型制药企业纷纷布局。”郑静进一步表示,“依托强大的研发团队和生物技术领域核心关键技术,信念医药是全球基因治疗新药领域,少有的与欧美跨国公司技术比肩的新创企业。”
BBM-H901注射液是信念医药拥有自主知识产权的AAV基因治疗药物,通过静脉给药将人凝血因子IX(Factor IX,FIX)基因导入血友病B患者体内,从而提高并长期维持患者体内凝血因子水平,以期达到“一次给药、长期有效”的治疗及预防出血效果。BBM-H901注射液药物的设计采用了拥有完全自主知识产权的肝靶向性血清型和高效基因表达盒,运用公司自主开发的无血清悬浮培养和层析工艺进行符合GMP要求的药物生产。BBM-H901注射液具有表达效果好、产量高、安全性强的特点。
BBM-H901注射液的基因治疗是国内最早开展临床试验的AAV基因疗法之一,自2019年就开始了研究者发起的临床研究(Investigator Initiated Trial, IIT, NCT04135300)。临床研究数据显示BBM-H901注射液具有良好的安全性和有效性,AAV基因治疗药物输注后患者体内凝血因子水平提高显著,并长期稳定,且在临床期间未发现明显的不良反应,患者的年化出血率(Annualized Bleeding Rate, ABR)显著降低。2021年4月,信念医药正式向国家药品监督管理局(NMPA)提交了BBM-H901注射液的临床试验申请(Investigational New Drug, IND)。2021年5月14日,药品审评中心(Center for Drug Evaluation, CDE)正式受理,并于2021年8月6日正式批准BBM-H901注射液进入临床试验阶段。
信念医药创办于2016年9月,是一家集基因治疗药物研发、生产和临床应用为一体的高科技企业,公司创始人为著名基因治疗行业领军人物肖啸教授。作为全球基因治疗行业资深专家,肖啸教授拥有超过35年的AAV基因治疗行业研发转化经验和深远的国际影响力,主持了20余项目国内外基因治疗研究项目,带领团队成功研发了数十种 AAV 基因治疗药物及相关的关键技术,其研究成果被美国《Discover》杂志评选为年度全球科学领域100项重大发现之一。肖啸教授也是全球基因治疗行业知名的连续创业者。2016年8月,其共同创办的Bamboo Therapeutics公司被辉瑞以6.45亿美元收购,药物目前已进入临床III期;2020年10月,其共同创办的Asklepios BioPharmaceutical 公司被拜耳以40亿美元收购,多个药物已进入临床阶段。

信念医药创始人肖啸教授
信念医药拥有数项全球领先的专利与技术,在靶向不同组织的AAV新型capsid、高效的转基因表达盒设计、先进的临床级载体制造工艺、创新的临床开发范式等领域进行了全面布局,已成功开发全球领先的HEK293 500L悬浮培养工艺和全层析的规模化下游纯化工艺,已有多个项目进入IND申报和临床验证阶段。公司研发管线包含血友病A、血友病B、帕金森症、老年黄斑变性、粘多糖贮积症、脊髓性肌萎缩症等多种适应症。
作为行业领先者,信念医药的研发实力获得顶尖投资机构的认可。截至目前,信念医药已经获得启明创投、礼来亚洲基金、夏尔巴、经纬中国、北极光创投、双湖资本、千骥资本、晨岭资本(CDG)等知名基金超1.5亿美元投资,公司已在美国北卡罗莱纳州,中国香港、上海、北京和苏州设立了办公室或研发、生产中心。
信念医药血友病基因疗法获临床试验许可,既是公司的里程碑事件,也将开启国内AAV基因疗法新篇章。依托领先技术,信念医药将持续通过AAV(腺相关病毒)载体技术为单基因遗传病、老年性疾病以及一些恶性疾病提供更加有效的创新性解决方案,以科技为信、以患者为念,助力全民健康。






 上一页
上一页